DIHS
Drug-induced hypersensitivity syndrome(DIHS)は、Drug reaction with eosinophilia and systemic symptom(DRESS)とも呼ばれ、 発疹、発熱、リンパ節腫脹、血液学的異常(特に非定型リンパ球出現や好酸球増多)、肝炎、腎炎、肺炎などの全身性疾患を特徴とする重篤な有害反応です。特定の薬剤を14日から60日間使用後に発症し、原因となる薬剤を中止しても、症状が持続することが特徴です。
歴史
DRESSと思われる最初の症例記述は、1937年にMyersらによって報告されました。米国デトロイトで淋病を患い、スルファニルアミドで治療された男性が、かゆみを伴う発疹を発症し、その後剥離性皮膚炎へと進行しました。その後、発熱、黄疸、好酸球増多症を発症しました。1950年には、ジフェニルヒダントインナトリウム使用後に倦怠感、吐き気、全身性筋肉痛を発症し、その後黄疸、発熱、発疹が起こり、剥離性皮膚炎や腹痛を伴うリンパ節腫症(非定型リンパ球・好酸球増多を伴う)に進行した症例が報告されました。DRESSという用語は、1996年にBocquetらによって、薬物過敏症に関するレビュー論文で最初に提案されました。歴史的には、類似の症状は「フェニトイン過敏症」、「抗けいれん過敏症」、「ダプソン症候群」、「ヒダントイン症候群」、「アロプリノール過敏症」と呼ばれてきました。1998年、日本の研究者たちはヒトヘルペスウイルス-6 (HHV-6)の再活性化を伴うカルバマゼピンおよびスルファサラジンによる薬物過敏症をDIHSと名付けました。これはウイルス再活性化と薬物誘発性アレルギーの関係を初めて論文化したものでした。
疫学
日本(全国疫学調査)では、2012 年の1 年間にDIHS で全国の病院を受診した患者数は約600 人で、発症率でみると人口100 万対4.5と類推されました。薬剤別の発症率は原因となる薬剤によって異なり、1/1000から1/10,000の範囲と報告されています。男女ともに年齢分布は40代から60代の間でピークを迎えます。原因と考えられる医薬品は比較的限られており、カルバマゼピン、フェニトイン、フェノバルビタール、ゾニサミド、ラモトリギン(抗てんかん薬)、アロプリノール(痛風治療薬)、トリメトプリム-スルファメトキサゾール(抗菌剤)、サラゾスルファピリジン(抗リウマチ剤)、ジアフェニルスルホン(抗ハンセン病薬・皮膚疾患治療薬)、 メキシレチン(不整脈治療薬)、ミノサイクリン(抗生物質)などです。日本の厚生労働省 重篤副作用疾患別対応マニュアル 薬剤性過敏症症候群(令和4年2月版)に誘因薬物の一覧が記載されています。

病因
DIHS/DRESSは主にT細胞を介して媒介される薬物、ウイルス、免疫系間の複雑な相互作用と考えられています。薬剤が免疫応答を刺激しDIHS/DRESSを引き起こすモデルはいくつかありますがここでは2つのモデルを紹介します。
文献5】より
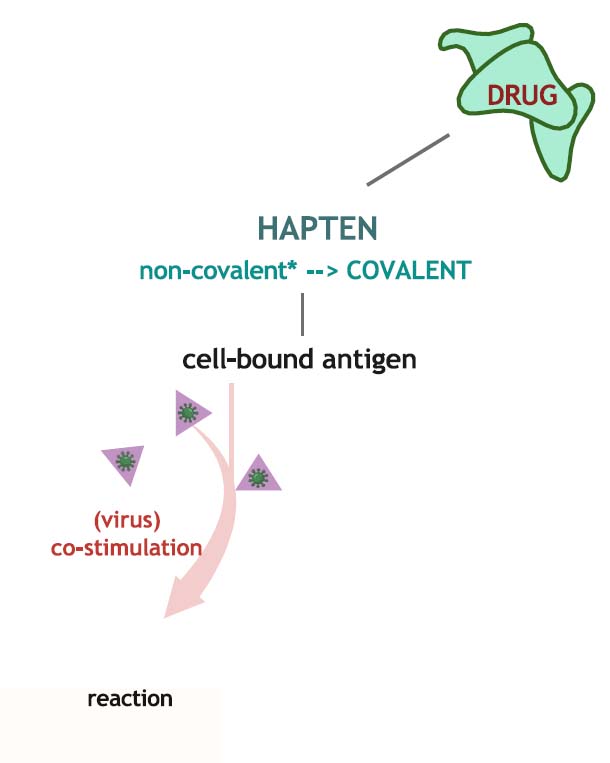
ハプテンモデル
薬剤は通常抗原として直接作用するには小さすぎますが、タンパク質に結合することで特異的な免疫応答を開始します。薬物は主にタンパク質に非共有結合で結合しますが、一部の薬剤(例:ペニシリン)は、共有結合することもあります。これらの薬剤はハプテンと呼ばれ、安定したハプテン・タンパク質複合体を形成し、新たな抗原として機能し、薬剤特異的抗体やT細胞反応を引き起こすことがあります。しかし、これらの新しい抗原は、共刺激がないため免疫系では通常無視されます。ただし、薬物投与時にウイルス感染などの他の免疫活性化が起こると、ハプテン・タンパク質複合体による紅斑などの臨床症状を伴う免疫反応が起こることがあります。
文献5】より
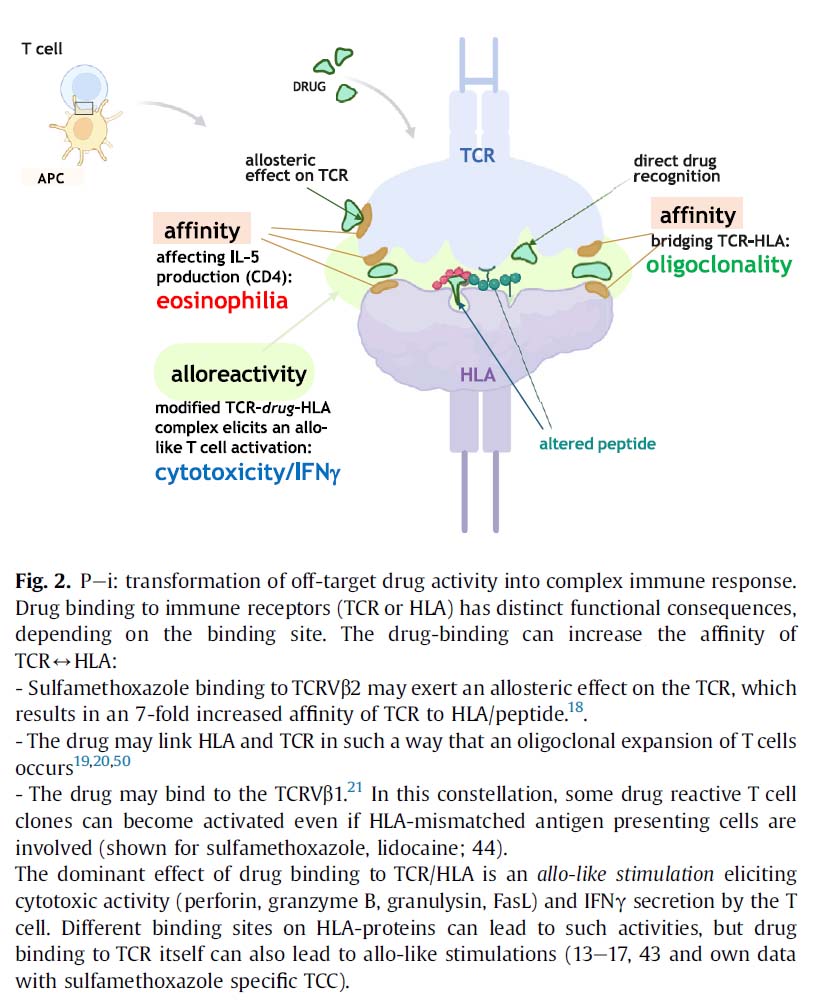
免疫受容体との薬理学的相互作用(pharmacological interaction with immune receptors:p-i)モデル
DIHS/DRESSなどの遅延薬物過敏反応は、主に薬物が直接的に免疫受容体であるHLAやT細胞受容体(T cell receptor:TCR)と非共有結合することにより、相互作用し、T細胞の活性化を引き起こすことが原因と考えられます。この反応は免疫受容体との薬理学的相互作用(pharmacological interaction with immune receptors:p-i)とも呼ばれます。p-i活性化は古典的な抗原によって活性化される免疫反応とは異なります。アレルギーとも異なります。
a) 薬物が免疫受容体であるTCR-HLAタンパク質に結合する事で、TCR-HLAタンパク質の構造変化が誘発され、自然免疫の関与なしに細胞毒性やIFNγ産生を伴うT細胞の刺激を誘発できます。
b) TCR/HLAへの薬物結合により、TCR-HLA相互作用の親和性を高めることができ、CD4+ T細胞のシグナル伝達やIL-5産生に影響を与え、 遅延薬物過敏反応によく見られる好酸球やオリゴクローナルT細胞の増殖に寄与します。
c) 抗原刺激とp-i刺激の両方が好酸球または好中球を豊富に含む炎症を引き起こすことがありますが、これらの刺激はその基礎的なメカニズムが異なるため区別されるべきです。
d) p-i活性化は、移植片対宿主反応と同様に、長期的なT細胞活性化を引き起こし、ウイルス血症、時折の自己免疫、または多剤高感受症を特徴とする新たな症候群を引き起こすことがあります。
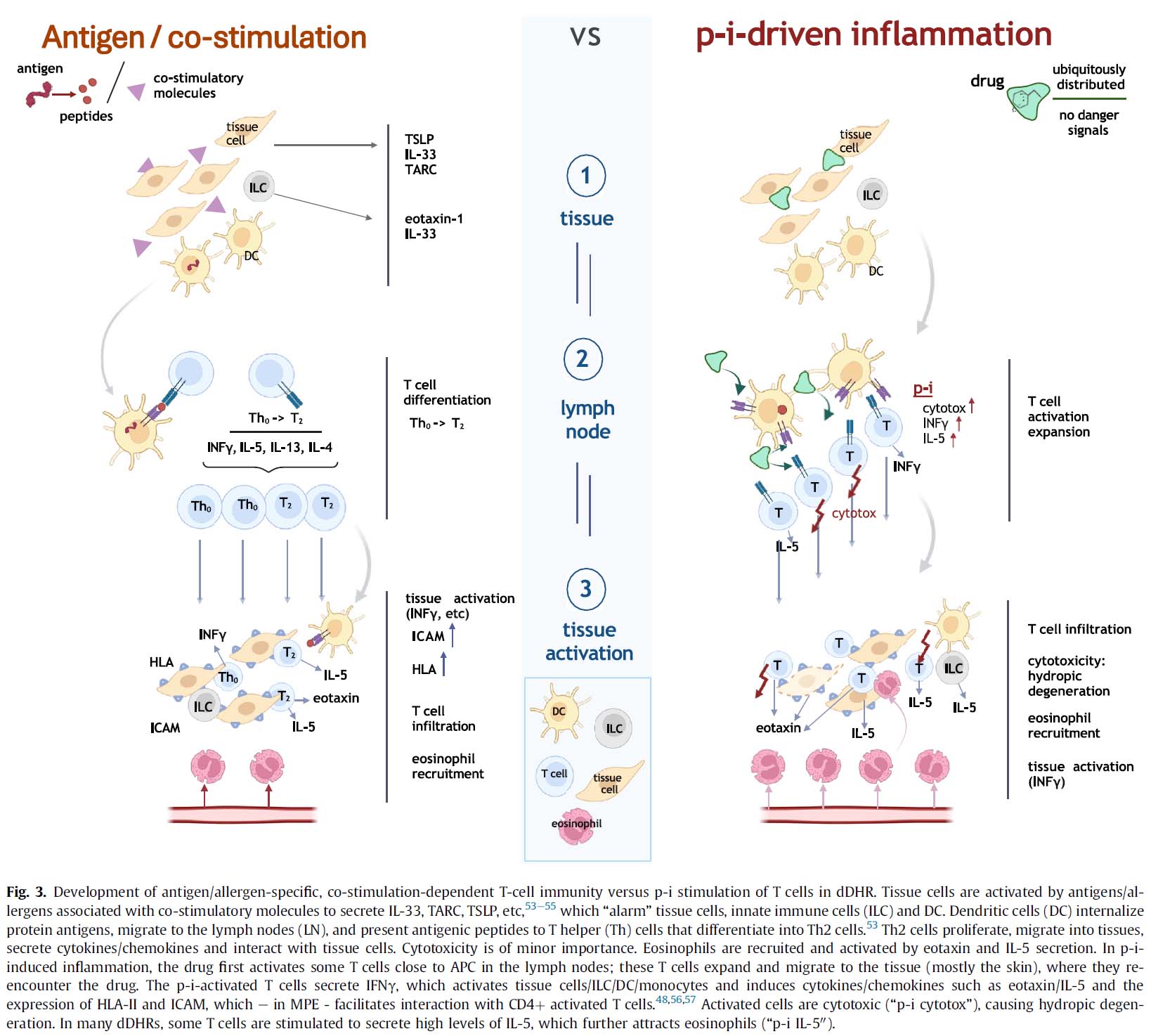
文献5】より
当初、遅延薬物過敏反応はハプテン・タンパク質複合体が新たな抗原として機能する抗原に誘発された免疫活性化と考えられていました。しかし、遅延薬物過敏反応患者における薬物に対する免疫応答の広範な解析により、ほとんどのT細胞活性化は別の経路から起因することが明らかになりました。薬剤が直接免疫受容体であるTCRまたはHLAに結合することが分かったのです。アバカビル、カルバマゼピン、ダプソン、バンコマイシンなどはHLAに結合し、スルファメトキサゾール、リドカインはTCRに結合することが知られています。遅延薬物過敏反応を引き起こす薬剤はTCRまたはHLAに結合することで、{TCR-ドラッグ-HLA}複合体が形成され、共刺激の存在なしに、T細胞にシグナルを発動させ、最終的に免疫活性を引き起こします。驚くべきことに、DIHS/DRESS患者には急性イベント後も何年も持続する活性化された末梢T細胞が存在します。これらT細胞は、薬物を中止してもp-i刺激により活性化され続ける可能性があります。p-i刺激は、遅発ウイルス再活性化や自己免疫の説明にもなり得ます。p-iでT細胞を刺激することで細胞増殖や強固な免疫応答が可能になります。増殖したT細胞は薬剤に(p-iを介して)反応しますが、そのTCRは特定の自己の免疫原性ペプチドと交差反応することがあり、自己免疫反応を引き起こすことがあります。DIHS/DRESS発症後数週間のウイルス血症は、一般的にウイルスの複製増加によって説明されます。あるいは、p-iで刺激された末梢T細胞が、特定のウイルス抗原(HHV-6, サイトメガロウイルス【CMV】など)に遭遇すると、細胞毒性活性が発現されます。これにより、感染組織細胞からウイルス放出され、ウイルス血症を引き起こす可能性があります。重度のDIHS/DRESSではp-i刺激により多剤高感受症(他の薬剤でも副作用発症)が生じることがあります。DIHS/DRESS患者の約25%が、化学的に異なる薬剤に対して別のDIHS/DRESSを発症します。in vitro解析は、活性化された表現型を持つT細胞が新薬への応答に関与していることを示唆しています。
HLA対立遺伝子
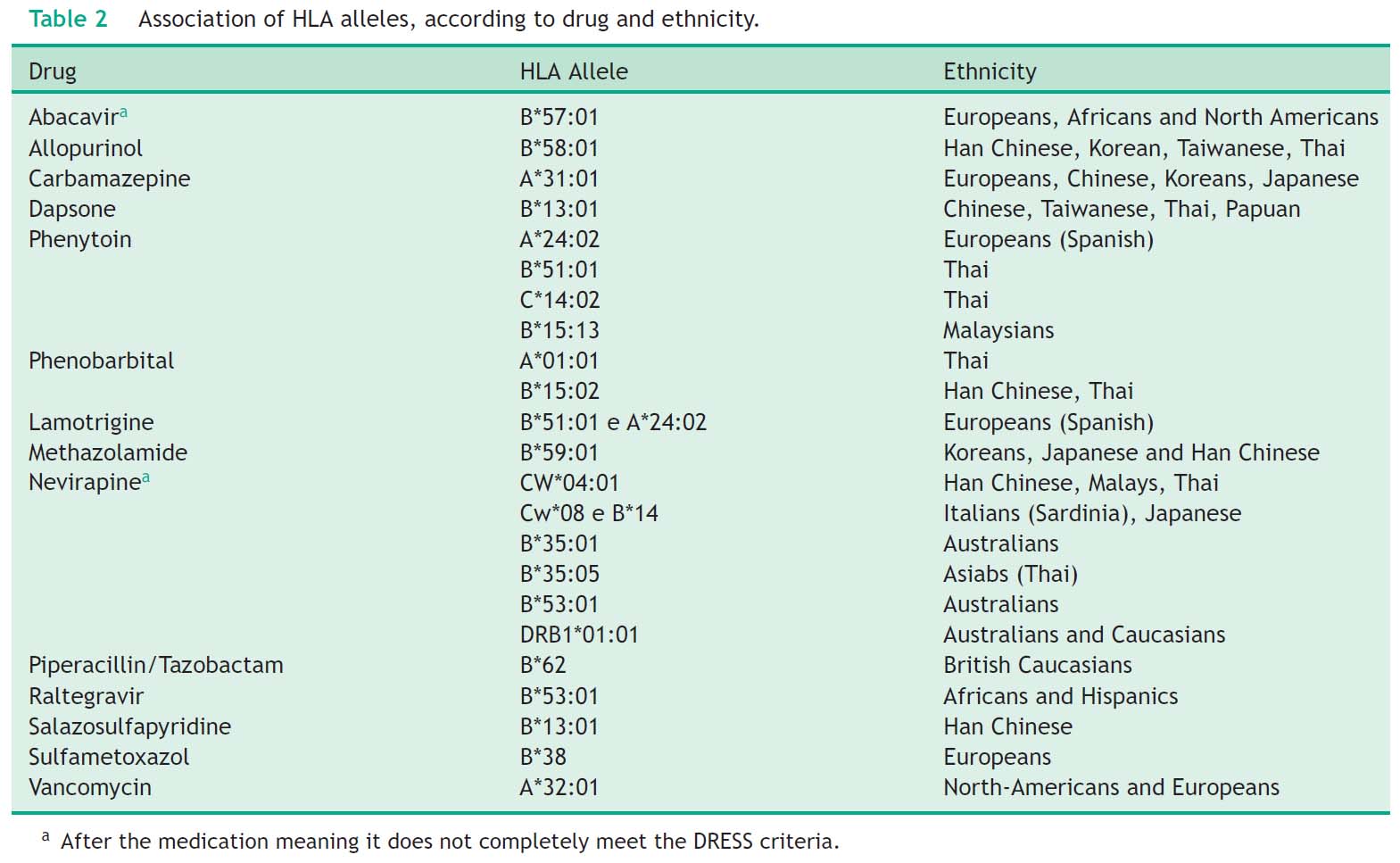
HLA対立遺伝子もDIHS/DRESS発症における最も関連性の高いリスク因子の一つです。下表のごとく、HLAのタイプが特定の薬剤と特定の民族に特異的であることが報告されています。理化学研究所のグループは2020年サラゾスルファピリジンやスルファメトキサゾール・トリメトプリムによるDIHSを含む重症薬疹患者においてHLA-A*11:01の保有率が高かったと報告しています。
文献3】より
症状
DIHS/DRESSはインフルエンザ様の倦怠感、咽頭痛、発熱、リンパ節腫脹の前兆から始まります。原因薬の投与から2〜3週間後に、発熱(38.5℃以上)や発疹が始まります。被疑薬中止3 日後程度から発熱や発疹などの症状の増悪を認めます。さらに、DIHS/DRESS患者では、治療目的として新たに薬を投与した場合、その薬剤に対しても交差反応を引き起こすことがよくあります。したがって、病気の経過中に新薬を投与する際は、たとえ原因となる薬剤と構造的に無関係であっても慎重な検討が必要です。
皮膚・粘膜の症状
皮膚の症状は多様(斑丘疹性発疹、多形性紅斑、湿疹、紫斑、膿疱性発疹、蕁麻疹、紅皮症など)で、体表の50%以上に影響を及ぼします。発症早期には特徴的な所見に乏しく、粟粒大程度の小型の丘疹、紅斑を散在性に認めます。紅斑は眼囲を避け眼周囲の蒼白が特徴的所見として挙げられます。その後、顔面浮腫 (76%)が出現し、顔面浮腫が悪化すると、目を開けにくくなり、重症の場合は気道閉塞を引き起こすことがあります。痒みはよく見られ、焼けるような痛みが出ることもあります。体幹や四肢の紅斑が拡大すると紫斑も出現します。下肢の紫斑の範囲は疾患の重症度と相関しています。DIHS/DRESSにおける膿疱性発疹は通常、耳、鼻、顎の周辺に見られます。
DIHS/DRESSの患者は、マイボーム腺機能障害、重度のドライアイを伴う眼表面疾患、結膜炎などの眼の症状も経験することがあります。粘膜の関与は最大56%の患者に認められます。しかし、通常は軽度で出血性がなく、スティーブンス–ジョンソン症候群/中毒性表皮壊死症とは区別されます。
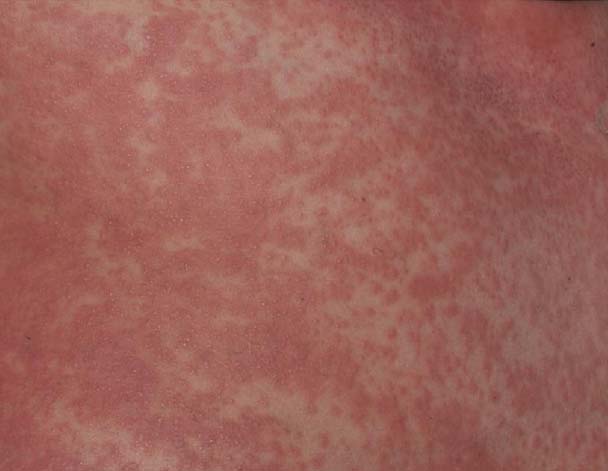
文献3】より
皮膚以外の症状
DIHS/DRESSの内臓病変は患者の最大91%に起こり得ます。肝臓の関与が最も一般的で、次いで腎臓と肺が続きます。リンパ節腫大は患者の50%から75%に発生します。肝障害の最も一般的な所見は肝酵素の上昇(胆汁うっ滞性、肝細胞性、混合型)です。場合によっては、肝不全に至ることもあります。
次に影響が大きい臓器は腎臓で、軽度の急性腎障害から重度の間質性腎炎まで様々で、重症例では永久的な末期腎疾患を引き起こします。DIHS/DRESSによる腎不全のリスクが最も高い患者は高齢者、既往の腎疾患、アロプリノール誘発DIHS/DRESS患者です。
肺は3番目に高頻度に影響を受ける臓器であり、間質性肺炎が最も一般的な症状です。ミノサイクリン誘発DIHS/DRESSでは肺障害の発生率が高いと報告されています。
心臓の障害は通常、心筋炎または心膜炎として現れ、初期症状から平均して70日かかります。一般的な兆候と症状は、呼吸困難、心原性ショック、胸痛、頻脈です。DIHS/DRESS患者は膵炎、大腸炎、胆管炎、脳炎/髄膜脳炎、血球貪食症候群、甲状腺炎などを発症することがあります。
検査所見
DIHS/DRESSでは、血液検査で通常白血球増多(>11,000/mm)、非定型リンパ球の出現(≥5%)、好酸球増多(≥1500/mm)、肝機能異常(ALT上昇:通常の2倍から5倍以上の範囲で変動)、腎機能異常(BUN、クレアチニン上昇、尿蛋白)、CRP高値を認めます。これらの異常は、DIHS/DRESSの初期段階では明らかでない場合もあります。しかし、被疑薬剤の中止後か病気の進行中に現れます。アロプリノールは腎障害の発生率が高いと報告されています。一方、ラモトリギンによるDIHS/DRESSは、軽度の白血球増殖症や肝異常を示す傾向があります。
急性期には血清IgGレベルが有意に低下しますが、回復期には徐々に正常値に戻ります。IgGが急激に増加する症例では、自己免疫疾患を合併に要注意です。血清TARCレベル(≥4000 pg/mL)の上昇は、DIHS/DRESSを他の薬物発疹と区別する重要なバイオマーカーとなります。TARCは強力なケモカインで、好酸球やCD4+およびCD8+ T細胞の皮膚への誘導を促進します。DIHS/DRESS患者のTARC値上昇は、HHV-6の再活性化および発熱、皮膚・粘膜病変、臓器機能障害などの症状の進行と相関しています。
薬剤誘発性リンパ球刺激試験(drug-induced lymphocyte stimulation test;DLST)は、薬疹症例の被疑薬同定のin vitro 検査として重要です。DRESS患者の後ろ向きの症例検討で、DRESS の回復期におけるDLST の感度および特異度は、それぞれ73%および82%であったのに対して,急性期ではそれぞれ40%および30%にとどまったことから、DLST 検査の施行時期は回復期が好ましいとされています。
組織所見
皮膚組織病理学的所見は多彩で、基底層の空虚化、リンパ球のエキソサイトーシス、角化細胞の壊死、血管周囲またはびまん性リンパ球浸潤、好酸球浸潤が見られることがあります。皮膚浮腫や赤血球の漏出、さらに偽リンパ腫性反応である海綿状疱疹、局所性表皮壊死が見られることがあります。
診断
DIHSの診断基準は日本皮膚科学会(Japanese Severe Cutaneous Adverse Reaction:J-SCAR)によって、DRESSの診断基準は欧州の学会(Registry of Severe Cutaneous Adverse Reactions:RegiSCAR)によってそれぞれ発表されました。これらの基準の重要な違いは、HHV-6再活性化がDIHSに含まれている一方で、DRESSには含まれていないことです。


文献1】より
重症度スコア
DIHS/DRESS重症度スコア(DDS)スコアは、疾患の重症度を評価し、特に感染症および自己免疫合併症を予測するために開発されました。このスコアリングシステムは、CMVの再活性化や感染合併症のリスクがある個人を特定するのに有用です。臨床症状と検査結果に基づき、DIHS/DRESSの患者は軽度(スコア<1)、中等度(スコア1–3)、重度(スコア≥4)の3つのカテゴリーに分類されます。早期スコアリングは通常、初回症状発生から3日以内に実施され(early score)、フォローアップスコアは2〜4週間後に評価されます(late score)。DIHS/DRESSの重症度の階層化は適切な治療を決定する上で不可欠です。
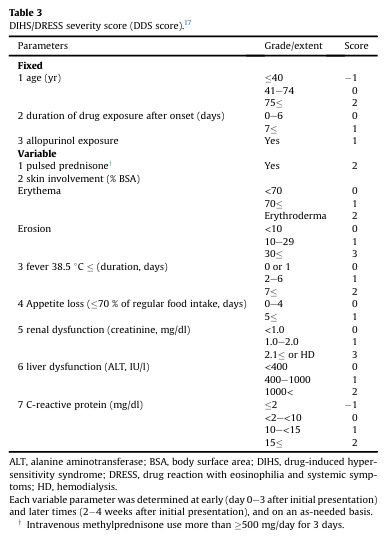
文献1】より
ウイルスの再活性化
HHV-6の再活性化
DIHSの特徴はHHV-6の再活性化であり、これは通常発症から3週間後(2~4週)に起こります。過去の研究では、ウイルス再活性化の連鎖反応はHHV-6またはEBV(ウイルスDNA検出中央値 HHV-6 23日、EpsteineBarr virus 【EBV】 24日)から始まり、その後HHV-7に続き、最終的にCMV(ウイルスDNA検出中央値 36日)に至ることが示されています。単純ヘルペスウイルスや水痘・帯状疱疹ウイルスなど他のヘルペスウイルスの再活性化も、DIHS/DRESSの期間中に認められることが報告されています。これらのウイルスのDIHSにおける連続的な再活性化は、感染合併症や自己免疫性合併症と関連しています。亜急性期におけるCMV再活性化は致命的な合併症を引き起こす可能性があります。一方、HHV-6およびEBVの再活性化は自己免疫性合併症と関連していることが多いです。適切なタイミングで検査すれば、ほとんどのDIHS患者でHHV-6再活性化が検出されます。HHV-6の存在は、HHV-6 IgG抗体レベルを測定し、ペアの血清サンプルが4倍以上増加することを観察することで確認できます。血液サンプル(全血またはリンパ球)のポリメラーゼ連鎖反応(PCR)解析は、HHV-6の再活性化を検出する効果的なツールであることが証明されています。唾液PCRアッセイもHHV-6再活性化を特定するための有用なツールとして報告されています。皮疹の悪化や検査異常は、原因薬が中止され、全身性コルチコステロイドが開始された後、数日から数週間後に起こることが多いですが、この増悪はヘルペスウイルスの再活性化によって引き起こされると考えられています。
CMVの再活性化
ヘルペスウイルスの中で、CMVの再活性化は致死的な合併症を引き起こす可能性があるため特に懸念されています。CMVの再活性化は抗原血症(例:C7-HRPおよびC10/C11)やPCR解析による白血球内DNA検出(10個あたり≥20ゲノム)によって確認できます。以前の後ろ向き研究では、CMV-DNAまたは抗原血症は初発症状出現後平均27.2日(範囲:16〜45日)で検出されました。CMV再活性化を伴うDIHS/DRESS患者は、腎障害(クレアチニン ≥1.0 mg/dL)、肝機能障害(ALT ≥400 IU/L)、CRP値の上昇(≥10 mg/L)、血小板減少症などが頻繁に観察されます。DDSスコアは、CMV再活性化などの感染性合併症の発症を予測するのに役立ちます。
合併症
DIHS/DRESS患者の約15%〜25%が合併症を発症します。これらは主に感染性合併症と自己免疫性合併症の2種類に分類されます。感染性合併症は通常急性期および亜急性期(発症後約30日)に発生し、自己免疫性合併症は発症から3か月以上経過した回復期に現れます。

文献1】より
感染性合併症
感染性合併症には、MRSAによる肺炎、CMV肺炎、ニューモシスチス肺炎、敗血症、脳炎、CMVによる消化管出血が含まれます。2018年の研究では、CMV再活性化を受けたDIHS/DRESS患者の45%がCMV関連合併症を発症し、そのうち60%が致命的な結果をとなっていました。
自己免疫性合併症
全身性コルチコステロイド治療終了後もDIHS/DRESSの回復期に自己免疫性合併症が発症することがあります。したがって、長期フォローアップが不可欠です。以前の研究では、3〜10年間追跡した患者で自己免疫性合併症の発症率が約16%でした。抗核抗体、抗甲状腺ペルオキシダーゼ抗体、抗DNA抗体などの自己抗体陽性は、自己免疫性合併症の出現より約8年前に認められていました。自己免疫性合併症には自己免疫性甲状腺炎、円形脱毛症、尋常性白斑症、関節リウマチ、全身性エリテマトーデス、全身性硬化症が含まれます。自己免疫性合併症発症のリスク要因は複数あり、ステロイドパルスまたは静脈内免疫グロブリン治療の使用、持続的なEBVまたはHHV-6の再活性化などが含まれます。平均して、自己免疫性合併症は平均5.7年(範囲:3〜18年)で発症する傾向があります。したがって、DIHS/DRESS患者は自己免疫疾患への進行可能性を評価するために少なくとも3年間の経過観察が必要です。特に静脈内免疫グロブリンまたはコルチコステロイドパルス療法で治療された患者には、連続的なモニタリングが推奨されます。
治療
DIHS/DRESS管理の最初のステップは、早期DDSスコアを用いて疾患の重症度を評価することです。軽度の場合は局所コルチコステロイドを含む支持療法で十分です。中等症以上では、全身性コルチコステロイドは第一選択の治療法であり、疾患の重症度に応じて0.5~1 mg/kg/日投与されます。全身性コルチコステロイドの減薬は、疾患の重症度に応じて6〜8週間かけて徐々に行うべきです。一般的には1〜2週間ごとに5〜10mgずつ徐々に減量することが推奨されます。DIHS/DRESSに対するコルチコステロイドのパルス療法は議論の的であり、通常は炎症や難治性疾患を伴う重症例に用いられます。過去の研究では、パルス療法で治療された患者はしばしばCMVの再活性化が起こり、高い死亡率が報告されていました。さらに、パルス治療を受けた患者では自己免疫性合併症が多いことが明らかになりました。したがって、パルス療法は慎重に検討されるべきです。DIHS/DRESS の経過中には多剤薬剤感作を引き起こすことが多いため、発熱に対するNSAIDs、抗菌薬などの予防投与は可能な限り避けることが望ましいとされています。
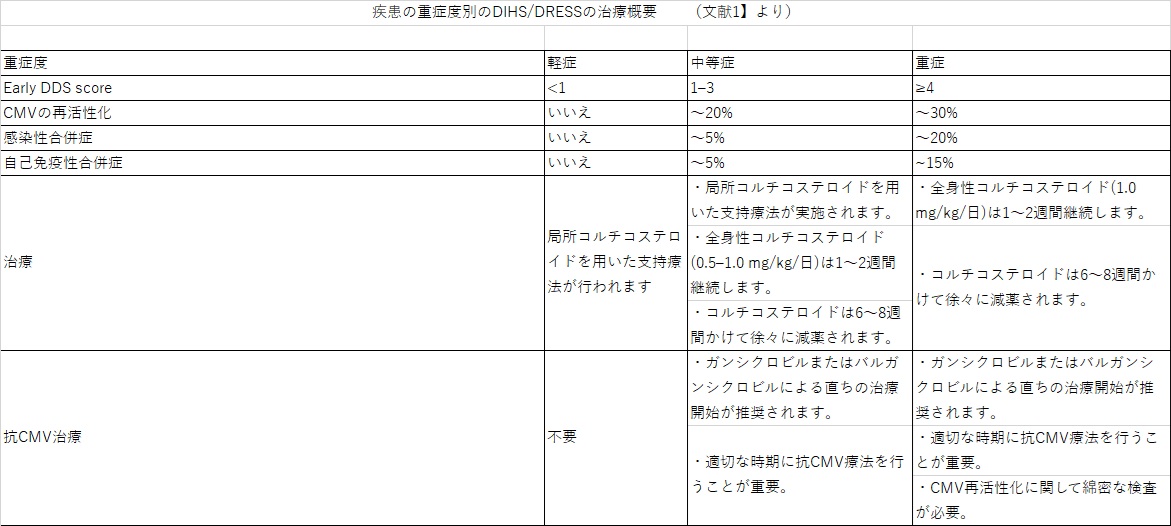
文献1】より
DIHS/DRESSの臨床経過管理において最も重要な点
1) 感染合併症の早期予測、
2) 感染に対する迅速かつ適切な治療、
3) 回復期における自己免疫合併症の予測、
4) 自己免疫合併症発症リスクの高い患者の長期追跡。
CMV治療
DIHS/DRESS治療の主な目的は、CMVの再活性化に対応し、その後の重篤な合併症の発症を防ぐことです。コルチコステロイドの使用中では、CMVの再活性化などの合併症リスクを高める可能性があります。重症症例ではコルチコステロイド投与を行いながら、CMVの再活性化をモニターし、再活性化が判明したら即座に抗ウイルス治療が必要です。ガンシクロビルやバルガンシクロビルなどの抗CMV療法は、CMV検査の改善が確認されるまで継続すべきです。以前の分析では、抗CMV治療を受けたCMV陽性患者の死亡率は22%であり、抗CMV治療なしの50%に比べ有意に低かったです。CMVの再活性化を検出してから抗CMV療法開始が3日以上遅延すると、重篤な合併症を引き起こします。まとめると、CMV再活性化後の抗CMV療法の早期開始と長期投与は、致死的な合併症の予防と死亡リスクの低減に不可欠です。
第二選択治療
重症DIHS/DRESS患者の中には、ステロイド耐性DIHS/DRESSと呼ばれる全身性コルチコステロイドに良好な反応が見られず、ステロイド減薬中に再発を経験する方もいます。このようなケースや全身ステロイドの禁忌がある患者、重度のステロイド関連副作用がある患者では、第二選択治療が必要となります。シクロスポリン、ミコフェノール酸モフェチル、静脈内免疫グロブリン療法、生物学的製剤(IL-5/IL-5R阻害剤、IL-4/IL-13阻害薬)、JAK阻害薬、血漿交換などが、第二選択治療の候補と考えられています。しかし、これらの治療法は症例報告や小規模後ろ向き研究などのデータしかなく、有効かどうかはまだ確定していません。今後はランダム化比較試験からのより高水準なエビデンスが必要です。
シクロスポリン
カルシニューリン阻害剤であるシクロスポリンは、T細胞によるIL-2産生の阻害を引き起こします。IL-2はT細胞活性化に不可欠であり、DIHS/DRESSにおける好酸球活性化に不可欠なIL-5の抑制も含まれています。これまでの報告は、主に症例研究および小規模サンプル数の後ろ向き解析のみです。シクロスポリンを単剤療法として1日2〜5 mg/kg投与した結果、平均治療期間は約16.8日で反応性が示されました。平均して、シクロスポリン開始後約4.1日で発熱と発疹の改善が見られ、効果的な効果が示されていますが、ウイルスの再活性化や再発を防ぐ役割についてはさらなる調査が必要です。しかし、韓国で行われた20年間の単一施設後ろ向き研究では、シクロスポリンとコルチコステロイドを比較した結果、入院日数(17.7日対14.9日)、治療期間(22.0日対20.4日)、臨床症状からの正常化までの時間において統計的に有意な差は見られませんでした。一方、最初に全身性コルチコステロイドで治療され、その後シクロスポリンに切り替えられた報告では、1〜3 mg/kg/日の低用量シクロスポリンでも良好な効果が示されており、シクロスポリンが全身性コルチコステロイド療法の効果的な代替または補助療法となる可能性を示しています。
ミコフェノール酸モフェチル
ミコフェノール酸モフェチル(MMF)は、リンパ球を選択的に標的として、抗体形成を阻害し、リンパ球および単球の内皮細胞への接着を減少させることで、白血球の炎症部位への遊走を妨げる免疫抑制剤です。報告はあまり多くありませんが、MMFはDIHS/DRESSの治療に用いられています。例えば、DIHS/DRESSの後遺症として激痛性心筋炎を患っていた28歳のアフリカ系アメリカ人女性は、コルチコステロイドのパルス療法、静脈内免疫グロブリン療法、MMFの併用療法で症状が改善しました。さらに、14歳のDIHS/DRESSの少女に対しては、コルチコステロイドを減量目的で1日2回500mgのMMFを追加したところ、効果的に治療されました。持続性リンパ球性心筋炎を伴うミノサイクリン誘発DIHS/DRESSの症例では、急性期からの寛解後の維持療法として、MMF 1500mg、プレドニゾン15mgを併用されました。したがって、これらの症例はMMFがDIHS/DRESSの寛解期における補助的維持療法として機能しうることを示唆しています。MMFの免疫抑制効果を考慮すると、感染性合併症や悪性腫瘍の可能性について、長期の高用量投与が必要な場合は慎重にfollow upする価値があります。
静脈内免疫グロブリン療法(IVIG)
免疫グロブリンは、数千人の献血者から集めたポリクローナル血清IgGの製剤です。IVIGのDIHS/DRESSに対する治療メカニズムはまだ完全には解明されていませんが、免疫調節、抗炎症活性、ウイルスの中和作用が関与する可能性があります。複数の症例報告では、コルチコステロイド難治性DIHS/DRESS治療として、全身性コルチコステロイド併用しながら3〜5日間連続でIVIGにて、臨床症状の迅速な改善とステロイドの減量が認められています。一方、重度の感染を合併しているため、ステロイドの禁忌のDIHS/DRESS患者に対しIVIG単剤治療が成功した例もありますが、有効ではなかったという報告もあります。興味深いことに、IVIGのタイミングはDIHS/DRESSの治療において重要な役割を果たす可能性があります。DIHS/DRESSの初期および急性期において、コルチコステロイド治療群では自己免疫疾患の発症率が有意に低く、一方、IVIG単独投与群では自己免疫疾患の発症率が有意に高いことが報告されています。IVIGがB細胞の回復を加速させ、さまざまなエピトープに特異的に反応する自己反応性B細胞の拡張し、自己抗体の生成や自己免疫疾患の発症に寄与します。これらの発見に基づき、DIHS/DRESS患者におけるIVIG単独療法は推奨されず、IVIGのタイミングにも議論の余地があります。IVIGは低免疫グロブリンレベルの補充、症状緩和、ステロイド減量の補助療法として有用である可能性があると考えられます。
IL-5/IL-5R阻害剤
IL-5は、IL-33、TARC、TGF-β、胸腺間質リンパ生成素(thymic stromal lymphopoietin)など他のケモカインと相乗効果を有し、好酸球の遊走能、活性化、増殖、浸潤において中心的役割を果たし、好酸球炎症や組織損傷に寄与しています。DIHS/DRESS患者に対するIL-5/IL-5受容体に対するモノクローナル抗体治療例が、合計16例報告されています:メポリズマブ(抗IL-5) 7例、ベンラリズマブ(抗IL-5R) 7例、レスリズマブ(抗IL-5) 1例、DIHS/DRESSの治療経過中にベンラリズマブからメポリズマブに切り替えた例 1例。DIHS/DRESS患者に対するレスリズマブ、メポリズマブ、ベンラリズマブの単回投与または反復投与の有効性は決定的ではなかったが、ステロイドや他の全身免疫抑制剤と比較して副作用の発生率が低いことが示されました。したがって、抗IL-5/抗IL-5R生物製剤は、ステロイド耐性およびステロイド依存のDIHS/DRESS患者、さらにステロイド関連禁忌を持つ患者に対して、特に好酸球の有意な増加がある場合に新たな治療法を提供する可能性があります。
IL-4/IL-13阻害薬
IL-4、IL-5、IL-13などの豊富なサイトカインの上昇を特徴とするTh2型応答がDIHS/DRESSで観察されます。デュピルマブは完全ヒト型モノクローナル抗体で、IL-4およびIL-13の共有受容体成分をブロックできます。2件の症例報告では、デュピルマブ投与を外来治療のみ行い、皮膚症状と好酸球数が7日以内に改善したことが示されています。そのうち一例はプレドニゾン中止後5日後に再発し、その後デュピルマブ単独投与後に寛解を達成しました。別の一例の症状はプレドニゾン使用にもかかわらず悪化し続けましたが、デュピルマブの開始後に急速に改善しました。両患者ともデュピルマブ治療中止後2か月以内に軽度のリバウンド発疹を経験しましたが、再投与後は4か月以上寛解が維持されました。別の症例報告では、コルチコステロイド減量中に重度の再発を経験し、IgE値が上昇し、かゆみが顕著に現れました。その後、16週間のデュピルマブ投与によりコルチコステロイドの減薬が効果的に促進され、再発することなくIgE値の持続的な低下が維持されました。DIHS/DRESSの再発を防ぐためには、少なくとも6か月間デュピルマブの長期投与が必要であり、その適応例をより詳しく検討すべきです。
Janus kinase (JAK)阻害剤
Janus kinaseシグナル伝達および転写タンパク質活性化因子(JAK-STAT)経路の活性化により、IL-5、IL-6、IL-10、IL-13などのJAK-STAT依存性サイトカインが産生され、これらはDIHS/DRESSの病因に関与しています。心筋障害を伴う重度のDIHS/DRESS患者3例に対しJAK 1/3阻害剤トファシチニブ単剤療法が奏功した報告があります。トファシチニブ開始から24時間以内に、IL-5、IL-6、IL-13、C–C motif chemokine ligand 1 (CCL1)、CCL17、CCL22、好酸球数のレベルが急激に低下または正常化しました。トファシチニブに加えて、バリシチニブ、ウパダシチニブ、アブロシチニブなど他のJAK阻害薬がDIHS/DRESSで投与可能かどうかはさらなる研究が必要です。
血漿交換
DIHS/DRESSの病態生理には複雑な免疫反応に対するサイトカインストームが含まれているため、血漿交換がDIHS/DRESSの治療法として浮上しています。証拠は限られており、具体的なメカニズムは完全には解明されていません。ある報告では、生命を脅かす14歳のDIHS/DRESS患者が、高用量ステロイドの失敗後に合計4回隔日で行われた血漿交換によって劇的かつ持続的な臨床反応を示しました。さらに、53歳のDIHS/DRESS患者はステロイドパルス療法2回施行にもかかわらず2回再発を経験後、4回の血漿交換を受け、病状は改善し、コルチコステロイドの減量にも成功しました。血漿交換は急性腎不全および多臓器不全を伴う生命を脅かすDIHS/DRESSの管理において有望と見られています。
文献2】の著者らの推奨
1.) シクロスポリン、JAK阻害剤、IL-4/13阻害剤、IL-5阻害剤は大きな可能性を示します。
2.) IVIGはコルチコステロイドと併用した場合の感染リスクが高い場合に適応症とされています。
3.)血漿交換、その他の生物学的製剤(TNF-α阻害剤、抗IL-6受容体抗体、抗CD20抗体など)や免疫抑制剤(シクロフォスファミド、メトトレキサート、タクロリムスなど)の適用はケースバイケースで分析する必要があります。
予後
DIHS/DRESSの臨床コースは非常に多様です。一部の症例は全身性コルチコステロイドなしで被疑薬剤離脱後に完全に治りますが、一方では病気の経過中や回復後に感染症や自己免疫疾患などの重篤な合併症を発症し、死にいたるケースもあります。自己免疫性合併症として、自己免疫性甲状腺炎、1型糖尿病、自己免疫溶血性貧血、脱毛症などが、治癒後数か月から数年後に現れることがあります。DIHS/DRESS患者の死亡原因(推定死亡率は約10%)は微生物感染であり、肺炎(例:メチシリン耐性黄色ブドウ球球菌[MRSA]、CMV感染、ニューモシスチス肺炎)や敗血症が最も一般的です。DIHS/DRESSにスティーブンス–ジョンソン症候群や中毒性表皮壊死を合併した症例では致死率が高くなります。
サラゾスルファピリジン(SASP)によるDIHS/DRESS
2005年1月1日から2024年7月21日までに発表されたSASP誘発DRESS/DIHSに関する関連文献を、データベースを検索して収集しました。39名の患者(男性15名、女性24名)が研究に含まれ、中央値年齢は47歳(範囲:11〜82歳)でした。これらの患者のうち、30例(76.9%)が関節リウマチ、7例(17.9%)が潰瘍性大腸炎、1例(2.6%)が強直性脊椎炎、1例(2.6%)がクローン病と診断されていました。SASP投与後、DRESS/DIHSの中央値発症期間は28日(範囲:10〜60日)でした。これらの患者は、発熱(100%)、発疹(100%)、消化器系の反応(38.5%)、浮腫(35.9%)などの臨床症状を示しました。38名の患者で臓器病変が観察され、影響を受けた臓器は肝臓(94.7%)、リンパ節(78.9%)、腎臓(15.8%)、心臓(13.2%)、肺(7.9%)でした。全患者に血液学的異常が見られ、好酸球増多(69.2%)および非定型リンパ球症の出現(35.9%)が多く見られ、無顆粒球症(5.1%)、血球貪食症(5.1%)、汎細胞減少症(2.6%)も含まれていました。ウイルスの再活性化は21名(53.8%)で経験され、HHV-6(16例、76.2%)、HHV-7(1例、4.8%)、CMV(5例、23.8%)、EBV(2例、9.5%)、SARS-CoV-2(1例、4.8%)という結果でした。主な治療は、薬剤の即時中止と全身性コルチコステロイド投与でした。2名が死亡しました。
文献
1】Recent advances in the diagnosis and treatment of DIHS/DRESS in 2025. Allergology International 2025;74:372-379
2】The systemic treatments for drug reaction with eosinophilia and systemic symptoms (DRESS) beyond corticosteroids. World Allergy Organization Journal 2024;17:100935
http://doi.org/10.1016/j.waojou.2024.100935
3】DRESS syndrome: an interaction between drugs, latent viruses, and the immune system. Anais Brasileiros de Dermatologia 2025;100:104-120
https://doi.org/10.1016/j.abd.2023.12.010
4】厚生労働省 重篤副作用疾患別対応マニュアル 薬剤性過敏症症候群(令和4年2月版)
5】Delayed drug hypersensitivity reactions: How p-i transforms pharmacology into immunology. Allergology International 2025;74:33e41
https://doi.org/10.1016/j.alit.2024.08.006
6】薬剤性過敏症症候群診療ガイドライン2023. 日皮会誌 2024:134;559-580
7】Literature review of the clinical features of sulfasalazine-induced drug reaction with eosinophilia and systemic symptoms/drug-induced hypersensitivity syndrome (DRESS/DIHS). Front. Pharmacol. 2024;15:1488483.
doi: 10.3389/fphar.2024.1488483
<<2026年3月17日作成>>
関連ページ
- 関節リウマチの症状
- 関節リウマチの症状について説明します。
- 関節リウマチの検査
- 関節リウマチの検査について説明します。
- 関節リウマチの疫学、歴史
- 関節リウマチの疫学、歴史について説明します。
- 関節リウマチの病因
- 関節リウマチの病因について説明します。
- 関節リウマチの病態生理(関節炎)
- 関節リウマチの病態生理(関節炎)について説明します。
- 関節リウマチにおける細胞内シグナル伝達経路
- 関節リウマチにおける細胞内シグナル伝達経路について説明します。
- 関節リウマチとエピジェネティックス
- 関節リウマチとエピジェネティックスについて説明します。
- 関節リウマチの病因(関節外病変)
- 関節リウマチの病因(関節外病変)について説明します。
- 関節リウマチの治療
- 関節リウマチの治療について
- 抗リウマチ薬
- 抗リウマチ薬について説明します。
- メトトレキサート
- メトトレキサートについて説明します。
- サラゾスルファピリジン(SASP)
- サラゾスルファピリジン(SASP)について説明します。
- 生物学的製剤
- 生物学的製剤について説明します。
- JAK阻害剤
- JAK阻害剤について説明します。
- 関節リウマチ薬の内服の注意点Q&A
- 関節リウマチ薬の内服の注意点について説明します。
- リウマチ患者の日常生活上の注意
- 関節リウマチ患者が日常生活上で注意すべき点について説明します。
- リウマチとインフルエンザ
- 関節リウマチとインフルエンザについて説明します。
- ACR・コア・セット、DAS
- ACR・コア・セット、DASについて説明します。
- 関節リウマチと喫煙
- 関節リウマチと喫煙について説明します。
- 関節リウマチと脳心血管病変
- 関節リウマチと脳心血管病変について説明します。
- 関節リウマチと悪性腫瘍
- 関節リウマチと悪性腫瘍について説明します。
- 関節リウマチと妊娠
- 関節リウマチと妊娠について説明します。
- リウマチと災害
- リウマチと災害について説明します。
- 関節リウマチの手術
- 関節リウマチの手術について説明します。